关于干细胞培养上清液
由于受伤和老化等原因,我们的细胞每天都在受损。
而修复这些细胞的,就是自己分化成各种细胞并促进再生的“干细胞”。
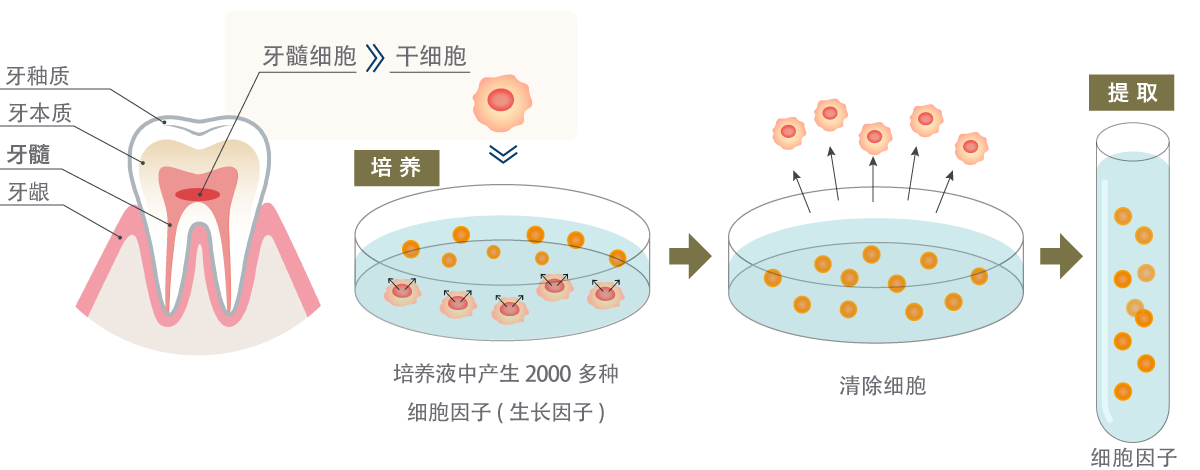
“干细胞培养上清液”是指培养干细胞时分泌的沉淀上层的透明液体。
它含有外泌体和细胞因子等数千种生长因子(生理活性物质),可期待其产生与干细胞相同的效果。
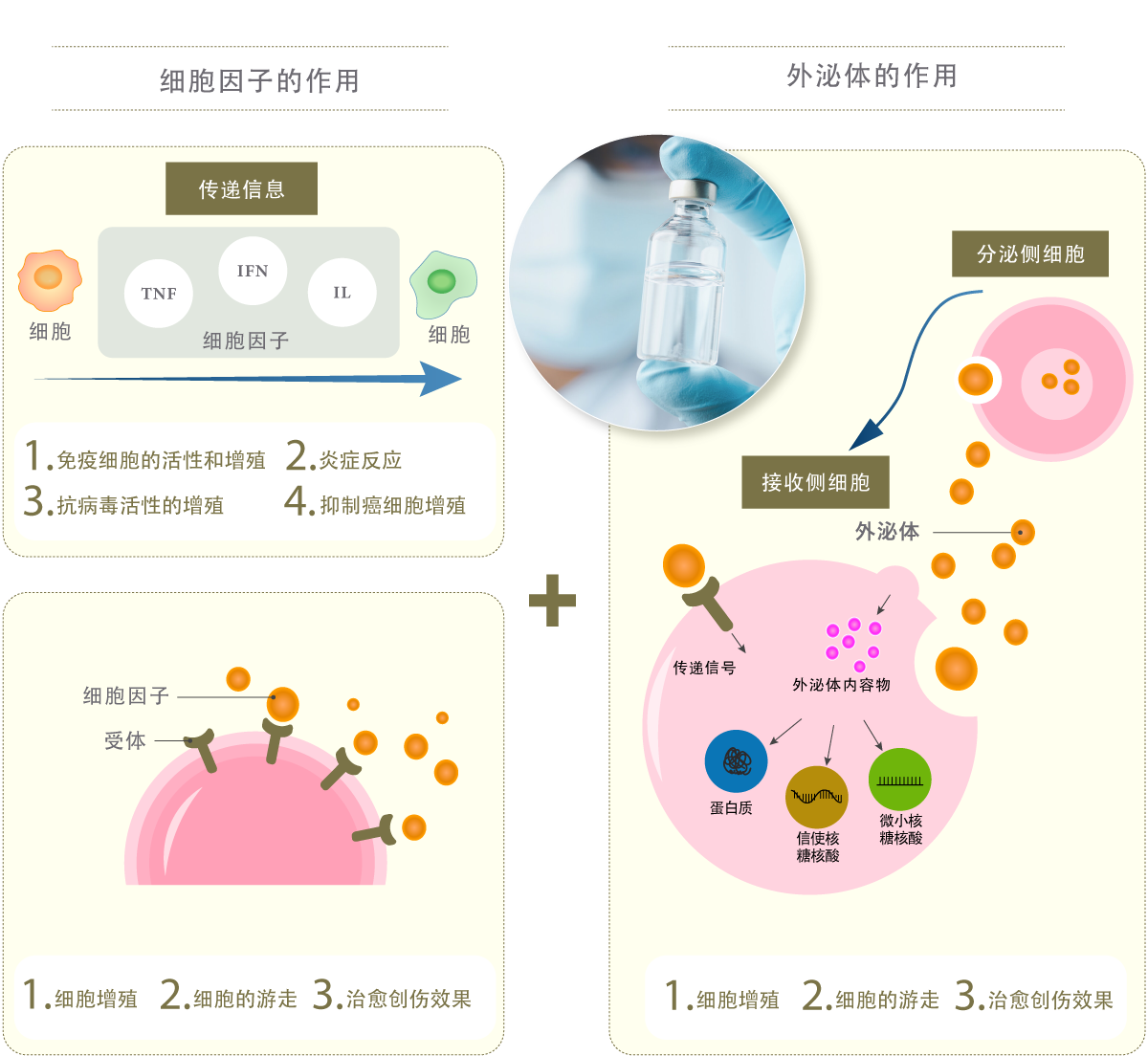
通过外泌体的作用,可期待细胞活性化、促进组织再生、改善血液循环等效果。
在抗衰老领域也备受关注,在来自脂肪、骨髓、脐带等各种人体组织由来的干细胞中,乳牙的牙髓干细胞含有最多的生长因子。
使用牙髓干细胞培养上清液(外泌体)的理由
牙髓的生长环境带来的优势
牙髓由坚硬的牙齿所包围。因此,与其他干细胞培养上清液相比,置于血液供给量非常少的恶劣环境中。正是因为置身于这样的环境中,所以才会生长为强而不易受损的细胞。
在这样的环境下生长的牙髓,活性能力非常强,细胞分裂和增殖能力也随之提高。增殖能力越强,外泌体和细胞因子的种类就越多,浓度也就越高。
本院的U-Factor®
本院与日本国内符合GMP标准的细胞加工中心合作,自主开发了外泌体(干细胞培养上清液),并将其命名为“U-Factor®”,并以点滴形式使用。
本院的“U-Factor®”,含有5000种以上细胞因子的蛋白质,同时含有高浓度的外泌体,是一种高品质的液体制剂。
本院的“U-Factor®”,含有5000种以上细胞因子的蛋白质,同时含有高浓度的外泌体,是一种高品质的液体制剂。
U-Factor® 四大要点
长持续性
可无限增殖,稳定持续的进行细胞供给。
含有丰富的生长因子和细胞因子
据报告称,与原代细胞相比,生长因子和细胞因子的含量约为原代细胞的30 ~ 50倍。
对复数细胞类型的效果
据报告称,其对多种细胞类型都有效果。可能对各种组织和器官的再生有帮助。
质量管理
使用在class100(Grade A)、class10,000(Grade B)的洁净室中生产的原料,通过了第三方机构在严格标准下的质量规格测试。
与细胞因子W组合的高细胞活性
在干细胞培养上清液的原液中,还含有从细胞中释放出的乳酸和氨等杂质。本院的“U-Factor®”,通过精制过程去除这些杂质。
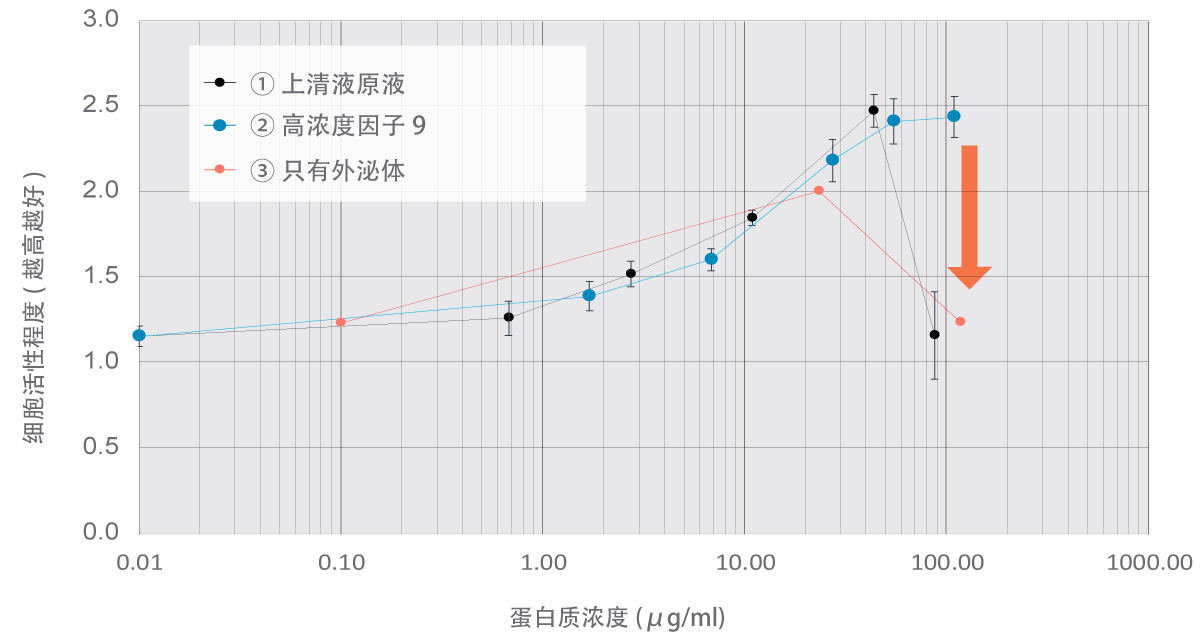
将干细胞培养上清液的原液,本院的U-Factor®,只有外泌体的提取液,这三种溶液改变浓度后进行细胞活性试验,发现U-Factor®比只有外泌体的提取液显示出更高的细胞活性。
将干细胞培养上清液的原液,本院的U-Factor®,只有外泌体的提取液,这三种溶液改变浓度后进行细胞活性试验,发现U-Factor®比只有外泌体的提取液显示出更高的细胞活性。
细胞活性试验内容及其结果
实验内容
- 干细胞培养上清液的原液
- U-Factor®
- 只有外泌体的提取液
实验结果
1的干细胞培养上清液原液和3的只有外泌体的提取液在高浓度时活性会急剧下降,这一点可以通过右侧图表(红色箭头)来确认。这应该是受到杂质影响的原因。另外,可以确认只有外泌体的提取液的活性程度也很低。本院的“U-Factor®”即使是在高浓度的情况下,细胞活性也会持续上升,这一点在实验中得到了验证。
细胞活性实验结果
没有明示实验结果的干细胞培养上清液和外泌体的点滴,有可能是没有进行杂质去除与浓缩的精制,或是没有进行细胞活性实验。
信赖性
我们使用来源明确的牙髓干细胞
本院的“U-Factor®”采集日本儿童脱落的乳牙,培养牙髓干细胞。 接受以人为对象的生命科学·医学系的研究不可缺少的伦理委员会审查,以最优程序进行拔牙及牙髓组织的采集。
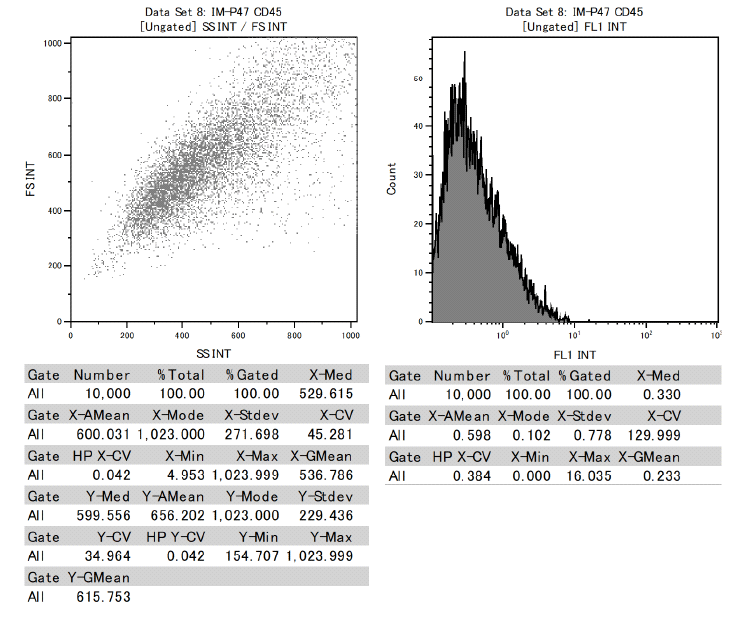
另外,确认牙髓干细胞在表示间充质干细胞的细胞表面标记中,CD73、CD90、CD105为阳性,CD34、CD45为阴性。
证明了这是具有分化成各种功能细胞能力的间充质干细胞。
表面标志物测试数据结果
CD73:Positive
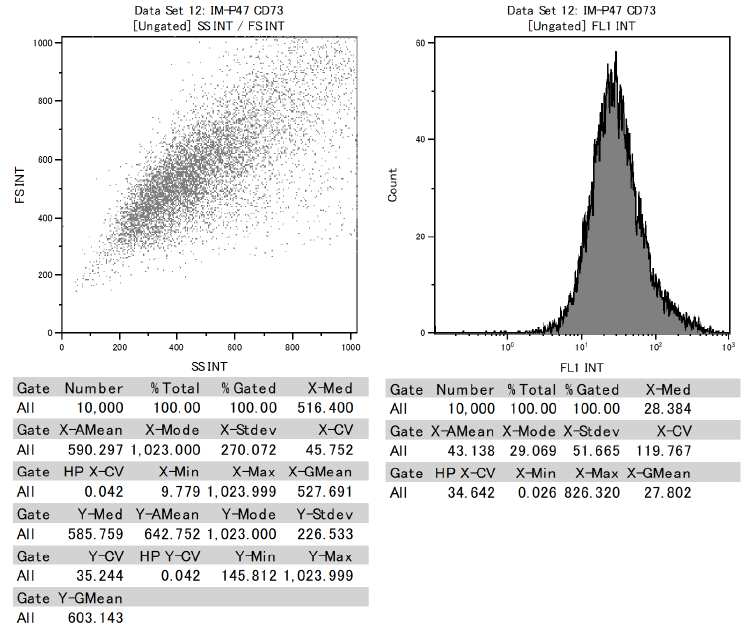
CD90:Positive
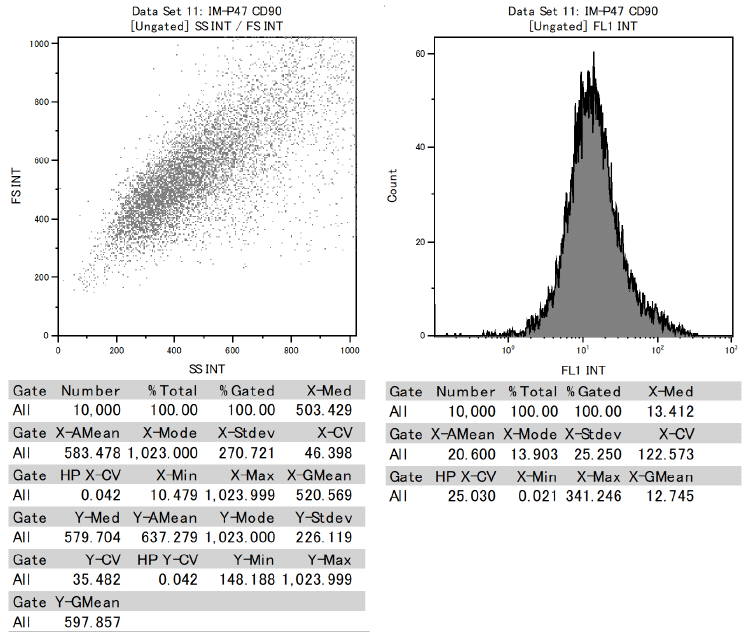
CD105:Positive
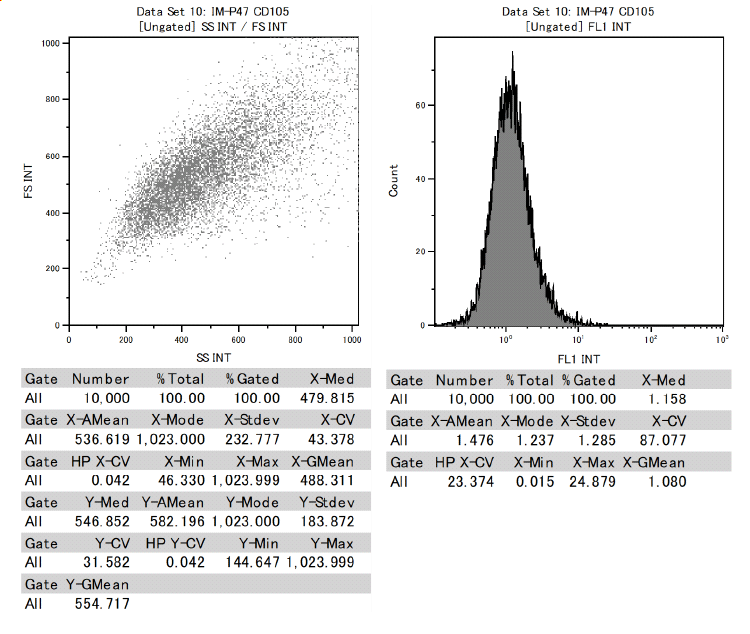
CD34:Negative
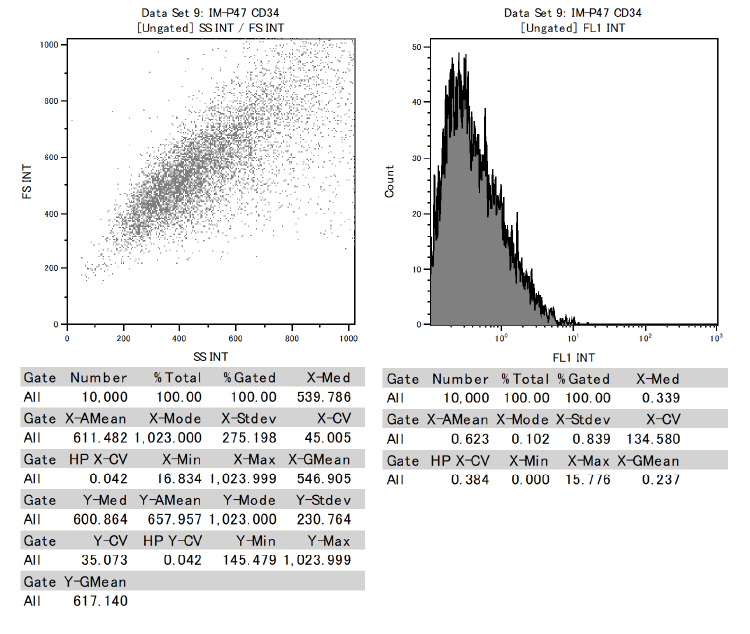
CD45:Negative
本院的“U-Factor®”一律不予使用来源不明确的牙髓干细胞,以及无法确认为间充质干细胞的干细胞。
在符合GMP标准的细胞加工中心严格生产
本院的“U-Factor®”是在遵守严格的药品生产质量管理标准GMP (Good Manufacturing Practice)的细胞加工中心生产的。除GMP之外,还遵守以下省令和标准指南。
符合省令
- GMP药品生产管理及质量管理标准
- GCTP再生医疗等产品的生产管理及质量管理标准
- GQP规定GQP药品、准药品、化妆品及再生医疗等产品质量管理方法的标准
- 关于确保再生医疗等安全性的法律
符合规格・标准指南
- ISOInternational Organization for Standardization (国际标准化机构)
规定各种质量规格的国际机构。 - ICHInternational Council for Harmonization of Technical Requirements for Pharmaceuticals for Human Use(药品管制协调国际会议)
全球范围内推广药品标准指南的国际机构 - MISEV2018是2018年国际细胞外囊泡学会(ISEV)发表的细胞外囊泡 (EV) 研究标准指南。

本院的“U-Factor®”一律不予使用在生产管理、质量管理、卫生管理等标准模糊的设施中所制造出的干细胞培养上清液及外泌体。
细胞接收时和产品出货时的检查
细胞加工中心在接收“U-Factor®”的基础细胞时,以及产品出厂时,都会分别进行安全性测试。在本院,只有通过那些测试的细胞才可用于“U-Factor®”。
细胞接收时的检查
根据厚生劳动省的生物原料标准(平成30年2月28日制定 厚生劳动省告示第37号),通过下述的安全性测试
- 无菌试验
- 内毒素试验/支原体试验
- 病毒否定试验(HBs抗原·抗体、HBc抗体、HTLV-I抗体(CLIA)、HIV抗原·抗体、梅毒(PRP/TPHA))
上清液出厂时的检查
- 无菌试验
- 内毒素试验/支原体试验
- 无细胞检查
通过4大安全性试验进行全面的质量管理
确认本院的“U-Factor®”在以下试验项目中全部为否定。
人类病毒试验
针对细胞加工药品质量及安全性指南中推荐的人类病毒(HBV/HCV/HIV/HTLV-I/HIV抗原·抗体/RPR/TPHA)进行试验。使用 NucleoSpin RNA 进行 DNA/RNA 回收程序的同时,从通过离心测试样本收集的细胞中提取核酸,对各病毒序列使用特异性引物/探针组合,通过反转录/实时PCR来判断病毒的存在。
无菌试验
对培养时增殖的霉菌等需氧菌,以及不需要氧气的厌氧菌进行测定。使用无菌试验装置细菌警报系统,在试验培养基接种试验样本后,在32.7℃条件下培养7天,从细菌的增殖性判定其无菌性。另外,作为阻碍确认试验,在试验培养基接种试验样本和各种标准菌,并进行与试验样本同样的培养。标准菌种也在生长,由此判定没有阻碍。
支原体否定试验
支原体是具有自我增殖功能的最小的微生物,在生物学上被分类为细菌,因能引起肺炎等而广为人知。因为细菌太小且没有细胞壁,很难观察,因此使用MycoSEQMycoplasma Detection Kit,从样本及样本加阳性对照DNA中提取DNA,使用支原体特异性引物,通过实时PCR方法判断支原体的存在。
内毒素试验
内毒素是一种致热原(发热性物质),具有发热作用、致死毒性等生物活性。Endosafe-PTS试剂盒JP中添加样本,用内毒素测定装置进行测定,以加入试剂盒中的内毒素对照品为指标,对内毒素试验对照品的添加回收率和样本的内毒素试验浓度进行测定。
极纯的外泌体上清液“U-Factor®”
本院的“U-Factor®”是在浓缩过程中无限去除氨和乳酸等杂质的精品,因此是高纯度的外泌体上清液。
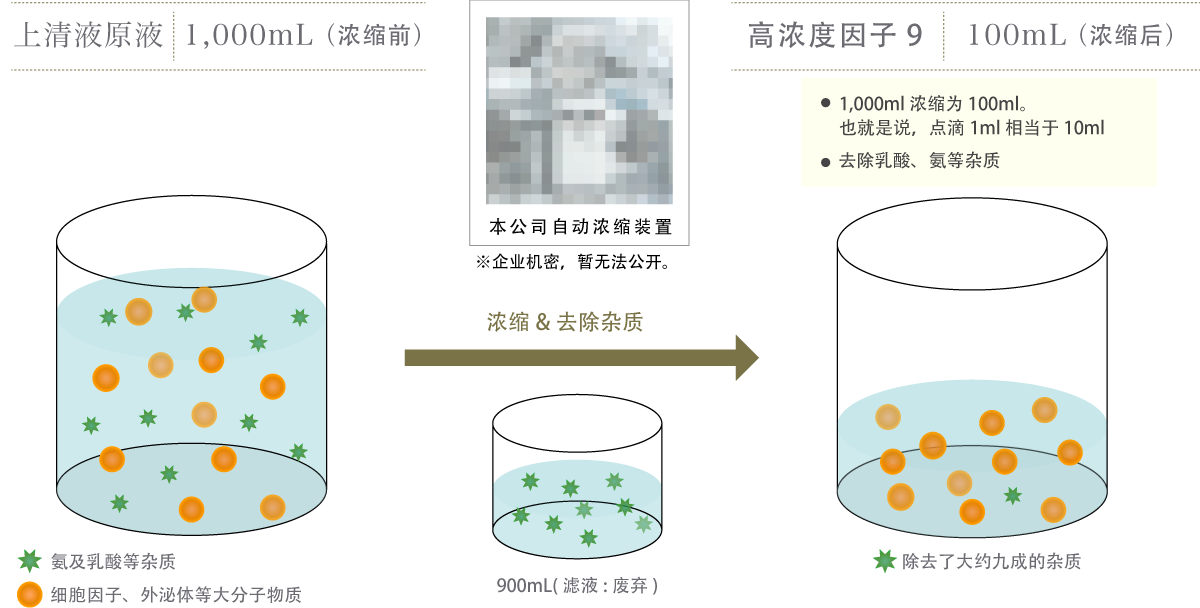
去除杂质需要消耗时间和专业知识。未经处理的原液,杂质浓度高,质量不好的原液,如果体内点滴回输有可能引起副作用,因此本院不予使用。